�v���X�����[�X
���l�s����w
�|�V�~�����[�V�����Ǝ����̃R���{�ɂ���������̋@�\�𖾁|
�T�v�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�@�����w�������i�����j������Ȋw�����Z���^�[�Ɖu�P�퐫�����`�[���̏H�R�אg�`�[�����[�_�[�A�L�b�Z�C��i�H�Ɗ�����Ђ̊ێR�S�Ǝ�C�i����������Ȋw�����Z���^�[�Ɖu�P�퐫�����`�[�����C���i���������j�A���l�s����w��w�@������Ȋw�����ȖƉu�����w��������w�@���i���������j�j�A�}�g��w��w��Ìn������Ȋw��P�~�J���o�C�I���W�[IT�n�����̍L��M��������̋��������O���[�v�́A�V���ȖƉu�}��������KSI-6666�����A���̖������������@�\�肵�܂����B
�@�{�������ʂ́A���ȖƉu����[1]�̎��ÂɌ��������i�̊J���ɍv������Ɗ��҂ł��܂��B
�@���ȖƉu�����ł́A�Ɖu�זE�̈��T�����p��[2]�������ֈړ����ėL�Q�ȖƉu�����������N�����܂��B����A���������O���[�v�́AT�����p���̈ړ���}������ᕪ�q������KSI-6666��V���ɓ��肵�܂����BKSI-6666�̖���͎������������A��������������i�ɔ�ׂĕ���p�����Ȃ����Ƃ��������܂����B�܂��A�v�Z�Ȋw�ɂ��V�~�����[�V�����\���ƌ��؎����ɂ��AKSI-6666�̖���̎�������������郁�J�j�Y�����𖾂��܂����B
�@�{�����́A�Ȋw�G���wNature Communications�x�I�����C���Łi7��19���t�F���{����7��19���j�Ɍf�ڂ���܂����B
[�摜1]https://digitalpr.jp/simg/1706/91833/700_249_2024071813292666989a262ca98.jpg
�������������V�����Ɖu�}��������KSI-6666
�w�i�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�@���ȖƉu�����́A���Ȃ̑g�D�ɑ��ĖƉu�������N���鎾���ł��B���̍ہAT�����p���̓����p�g�D����Ɖu�������N�������Ȃ̑g�D�Ɉړ����ď��Q��^���܂��B����T�����p���̈ړ��ɂ́A�X�t�B���S�V��1-�����_���Z�v�^�[1�iS1PR1�j[3]���K�v�ł��B�܂�AS1PR1�̋@�\��j�Q����AT�����p���̈ړ���}���邱�Ƃ��ł��A���ȖƉu�������}������܂��B���̂���S1PR1�̍�p��}�����鉻�����iS1PR1���ߖ�j���J������A���ȖƉu�����̎��Ö�Ƃ��Ďg���Ă��܂��B
�@����܂ł�S1PR1���ߖ�́AT�����p�������łȂ��S���̍זE�ɂ��e�����邽�߁A����p�Ƃ��ď���[4]�������N�������Ƃ����ƂȂ��Ă��܂��B���̕���p�́AS1PR1���ߖ�S1PR1�Ɍ�������ہA�ꎞ�I��S1PR1��“������”���邱�Ƃ������ł����B���̂��߁AS1PR1��S�������������Ȃ�S1PR1���ߖJ������܂������A���̑����͖�������������Ȃ��̂����_�ł����B
������@�Ɛ��ʁ@
�@����A���������O���[�v�́A����܂ł̒m�����Q�l�ɉ������X�N���[�j���O���s���AS1PR1�̍�p��}������V�����������Ƃ���KSI-6666�肵�܂����B��ʂɁAS1PR1���ߖ�𓊗^����ƌ��t���̃����p�����������邱�Ƃ���A�����p�����������Ă��鎞�Ԃ̒���������������̖ڈ��ƂȂ�܂��BKSI-6666�ł̓��b�g�̃����p���̌�����48���Ԉȏ㎝�����܂����B�����KSI-6666�́A���ȖƉu�����ł��鑽�����d����[5]�≊�ǐ�������[6]�̃}�E�X���f�������ŁA����܂ł�S1PR1���ߖ�Ƃقړ����̎��Ö���������Ƃ�������܂����i�}1�j�B�����āA�d�v�Ȃ��ƂɁA������S1PR1���ߖ�Ƃ͈قȂ�AS1PR1���ꎞ�I�Ɋ����������Ȃ����߁A�����̕���p������܂���ł����B���Ȃ킿�AKSI-6666�͊����̈��i�Ƃقړ��l�̖���Ǝ������������A����������p�̏��Ȃ�S1PR1���ߖ�ł���Ɣ������܂����B
[�摜2]https://digitalpr.jp/simg/1706/91833/600_261_2024071813292866989a28c961d.jpg
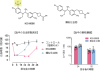
�}1 KSI-6666�̎����I�Ȗ���Ǝ��ȖƉu�����̎��Ð���
KSI-6666���^��̃��b�g���������p�����̌����i���j�Ƒ������d���ǃ}�E�X���f���i�����I���ȖƉu���]�Ґ����j�̕a�ԉ��P�i�E�j�B�R���g���[���͖Ȃ��Bp�͓��v�w�I�L�Ӎ��i�z�u���U���́j�B��\�I�ȃf�[�^�Ƃ��Ď������B
�@�����ŋ��������O���[�v�́AKSI-6666�̖�����������������@�\�̉𖾂ɒ��݂܂����B
�@�܂��AKSI-6666���ǂ̂悤�ȏ�Ԃ�S1PR1�ƌ������Ă���̂��ׂ邽�߂ɁAKSI-6666��S1PR1�̕��q�h�b�L���O�v�Z[7]���s���܂����B���̌��ʂ���\�������\���⌋���e�a���́A�������̂Ȃ����ߖ�ƂقƂ�LjႢ���Ȃ��AKSI-6666�̓����ł������̎������̐����ɂ͕s�\���ł����B�����ŁA���q���͊w�v�Z[8]�̈�ł��郁�^�_�C�i�~�N�X�@[9]��p���āAS1PR1�Ɍ�������KSI-6666���𗣂���ߒ����V�~�����[�V�������܂����i�}2��j�B���̌��ʂ���AKSI-6666�́A������������Ȃ�S1PR1���ߖ�i�ΏƖ�j�ɔ�ׁAS1PR1����𗣂��ɂ����A�Ɨ\�z���܂����B���ۂɁA��������KSI-6666��S1PR1����𗣂��锼�����i�𗣔�����[10]�j�𑪒肵���Ƃ���A9.41���Ԃł���A�������̂Ȃ����ߖ�̉𗣔������i0.2���ԁj�Ɣ�ׂĉ𗣂��x�����Ƃ��������܂����i�}2���j�B
[�摜3]https://digitalpr.jp/simg/1706/91833/600_600_2024071813293166989a2bebf37.jpg
�}2 KSI-6666��S1PR1����𗣂���V�~�����[�V�����ƌ��؎���
���q���͊w�V�~�����[�V�����ɂ��AKSI-6666�ƑΏƖ�̃X�t�B���S�V��1-�����_���Z�v�^�[1�iS1PR1�j����̉𗣓��Ԃ�\�z�����i��j�B���̂��̂̉�������ΐF�̖_�Ŏ������B�ΏƖ�͉~���ɉ𗣂��邪�AKSI-6666��S1PR1�̃��`�I�j���i����̍\���Ŏ������j�Ƒ��ݍ�p���邱�Ƃʼn𗣂��ɂ����B�V�~�����[�V�����ŗ\�z�����𗣓��Ԃ̈Ⴂ���A�|�{�זE��p���������Ŋm�F�����i���j�B��e�̂���̒��ߖ�̉𗣂̒��x�́A��e�̂̊������w�W�ɑ��肵���Bt1/2�͉𗣔������B
�@���ɁAKSI-6666��S1PR1����̉𗣂��x�������ׂ邽�߂ɁA�v�Z���ꂽ�𗣂̃V�~�����[�V�����ߒ����ώ@���AKSI-6666��S1PR1�̓��蕔�ʂ̃��`�I�j��[11]�Ƒ��ݍ�p���邱�Ƃʼn𗣂��ɂ����Ɨ\�z���܂����B�V�~�����[�V��������\�z���ꂽ���蕔�ʂ̃��`�I�j����KSI-6666�̑��ݍ�p�̏d�v�����������邽�߁A���`�I�j����ʂ̃A�~�m�_�ł���o����[12]�Ɋ�����S1PR1��|�{�זE�ɔ��������AKSI-6666�̉𗣂��������܂����B���̌��ʁA�\�z�ʂ�AKSI-6666�̓��`�I�j�����o�����Ɋ�����S1PR1���瑁���𗣂��邱�Ƃ��m�F�ł��܂����B
�@����ɁAKSI-6666��������̎�������S1PR1����̉𗣂��ɂ����Ƃ̊֘A���ׂ邽�߂ɃV�~�����[�V�����ߒ����ώ@���AKSI-6666�̕��q�\���Ɋ܂܂���̃x���[���i�}3���j�̂������[���̃x���[���ƃ��`�I�j�������ݍ�p���Ă���Ɨ\�z���܂����B�����ŁAKSI-6666�̃x���[���̒u�������菜�����������i�ގ��������j�ɂ��āAS1PR1����̉𗣂ׂ��Ƃ���A�𗣔�������0.98���Ԃł���AKSI-6666�i9.41���ԁj�Ɣ�ׂđ����𗣂��邱�Ƃ����炩�ɂȂ�܂����B���̉������̖���ׂ��Ƃ���A����̍ő劈���͂قڕς��Ȃ����̂́A48���Ԉȏ㎝������KSI-6666�ɔ�ׂāA�����Z�x���قړ����ɂ�������炸���������Ⴂ�i24���ԁj���Ƃ��������܂����i�}3���j�B
�@�ȏ�̌��ʂ���AKSI-6666�͖��[���̃x���[���ŁAS1PR1�̃��`�I�j���Ƒ��ݍ�p���邱�Ƃʼn𗣂��x���Ȃ�A���̌��ʂƂ��Ė������������ƌ��_�t���܂����B
[�摜4]https://digitalpr.jp/simg/1706/91833/600_424_2024071813293466989a2ea4a4a.jpg
�}3 �𗣂̑���KSI-6666�ގ��������̖��
KSI-6666�i����j���邢�͉𗣔������̒Z���ގ��������i�E��j�����b�g�ɓ��^��Ɍ����̔����������𑪒肵���i�����j�BS1PR1���ߖ�����b�g�ɓ��^����ƃ����p�����������Ĕ��������������邽�߁A���������������Ă��鎞�Ԃ̒���������������̖ڈ��ƂȂ�B�ގ��������̌����Z�x�́AKSI-6666�̌����Z�x�Ƃقړ����ł���ɂ�������炸�i�E���j�A�ގ��������̖���������́AKSI-6666�ɔ�ׂĒႢ�B
����̊��ҁ@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�@����܂ň��i�̖���̎������́A�̌����Z�x�Ő�������Ă��܂����B���Ȃ킿��ӂȂǂŌ������瑁������������i�͎��������Ⴂ�Ƃ̍l�����ł��B����A�{��������AKSI-6666�̎������ɂ́A��������̌������x�����łȂ��A�W�I�ł���S1PR1����̉𗣑��x���d�v�Ȃ��Ƃ����炩�ƂȂ�܂����B
�@�܂�A�����I�Ȗ���������i���J������ɂ́A�����Z�x�̌������x�̑���ɉ����āA�W�I�^���p�N������̉𗣑��x�̑�����d�v�ł��B�܂��A���q���͊w�𗘗p�����V�~�����[�V���������́A�𗣂̃v���Z�X��\�����邽�߂ɗL���Ȏ�i�ɂȂ�܂��B
�@�{�������ʂ́A���ȖƉu�����̎��ÂɌ��������i�̊J���֍v������ƂƂ��ɁA���ꂩ��̂��܂��܂Ȉ��i�J���ɂ�����d�v�Ȓm���ɂȂ邱�Ƃ����҂���܂��B
�_�����@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
���^�C�g����
Pseudoirreversible inhibition elicits persistent efficacy of a sphingosine 1-phosphate receptor 1 antagonist
�����Җ���
Yuya Maruyama, Yusuke Ohsawa, Takayuki Suzuki, Yuko Yamauchi, Kohsuke Ohno, Hitoshi Inoue, Akitoshi Yamamoto, Morimichi Hayashi, Yuji Okuhara, Wataru Muramatsu, Kano Namiki, Naho Hagiwara, Maki Miyauchi, Takahisa Miyao, Tatsuya Ishikawa, Kenta Horie, Mio Hayama, Nobuko Akiyama, Takatsugu Hirokawa and Taishin Akiyama
���G����
Nature Communications
��DOI��
https://doi.org/10.1038/s41467-024-49893-8
�⑫�����@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
[1] ���ȖƉu����
�Ɖu�n�����g�̐���ȍזE��g�D�ɑ��Ĕ������邱�ƂŁA�̂̋@�\�ُ�𗈂������̑��́B
[2] �����p��
�������̈��ŁA�ʏ�͕a���̂Ȃǂɉ������đ̂�h�䂷��ƂƂ��ɁA��x�N�����Ă����a���̂��L������B���t���ɂ͎��T�����p���AB�����p���A�i�`�������L���[�זE�Ȃǂ��܂܂��B���ȖƉu�����ł́A���T�����p����B�����p�������Ȃ̍זE��g�D�ɉ�������B
[3] �X�t�B���S�V��1-�����_���Z�v�^�[1�iS1PR1�j
�זE�\�ʂɂ����e�̃^���p�N���B���K���h�ł���X�t�B���S�V��-1-�����_���������邱�ƂōזE�ړ��Ȃǂ̍זE�����������N�����B
[4] ����
�S���̔������ُ�ɒx�����邢�͊Ԋu�������Ȃ�s�����B
[5] �������d����
�_�o���ۂ��Ă��鐑��i�������傤�j���ϐ��E�E�����邱�Ƃɂ��A�_�o�n�Ɉُ킪�N���鎾���B
[6] ���ǐ�������
�Ɖu�זE�����̍זE�ɉ������邱�ƂŒ��ɉ��ǂ𗈂������B
[7] ���q�h�b�L���O�v�Z
�������ƃ^���p�N���Ȃǂ̐��̕��q�̑��ݍ�p��\������R���s���[�^�V�~�����[�V�����B
[8] ���q���͊w�v�Z
�������\������X�̌��q�Ƀj���[�g���̉^����������K�p���āA���q�ʒu��G�l���M�[�̎��ԕω���ǐՂ����@�B
[9] ���^�_�C�i�~�N�X�@
�ʏ�̕��q���͊w�@�ł͓��B���ɂ�����Ԃւ̈ڍs��e�Ղɂ��邱�ƂŁA���ׂĂ̏�Ԃւ̃V�~�����[�V������Z���Ԃʼn\�ɂ�����@�B
[10] �𗣔�����
���K���h�ƃ^���p�N���Ȃnj���������Ԃ���A���҂��𗣂�����ԂɂȂ锽���ɂ����āA������Ԃ���������܂łɗv���鎞�ԁB
[11] ���`�I�j��
�^���p�N�����\������20��ނ̃A�~�m�_�̂����A�����������ł��Ȃ��K�{�A�~�m�_�̈�B�a�����A�~�m�_�ł��葤���ɗ������q���܂ށB
[12] �o����
�^���p�N�����\������a�����A�~�m�_�̈�B���`�I�j���ƈقȂ藰�����q���܂܂Ȃ��B
���������O���[�v�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�����w�������@������Ȋw�����Z���^�[
�@�Ɖu�P�퐫�����`�[��
�@�@�`�[�����[�_�[�@�@�@�@�@�@�@�@�@�@�@�H�R�אg�@�@�i�A�L���}�E�^�C�V���j
�@�@�i���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@�q�������j�@
�@�@�����X�`���[�f���g�E���T�[�`���[D�@�����@�q�@�@�i�����}�c�E���^���j
�@�@�i���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@���j
�@�@���C���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@���؉��T�@�@�i�i�~�L�E�J�m�j
�@�@�i���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@���j
�@�@�q���������@�@�@�@�@�@�@�@�@�@�@�@�@�ΐ열��@�@�i�C�V�J���E�^�c���j
�@�@�i���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@���i���������j�j
�@�@��w�@�����T�[�`�E�A�\�V�G�C�g�@�@�@�[�R�����@�@�i�n���}�E�~�I�j
�@�@�i���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@���j
�@�@�㋉�������@�@�@�@�@�@�@�@�@�@�@�@�@�H�R�L�q�@�@�i�A�L���}�E�m�u�R�j
�@�@�i���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@�q�������j
�@�@�Z�t�i���������A���@��b�Ȋw���ʌ������j�{���M�v�@�@�i�~���I�E�^�J�q�T�j
�@�@�e�N�j�J���X�^�b�t�T�@�@�@�@�@�@�@�@�{���^�I�@�@�i�~���E�`�E�}�L�j
�@�@�e�N�j�J���X�^�b�t�U�@�@�@�@�@�@�@�@�����ޕ�@�@�i�n�M�����E�i�z�j
�@�@�q���������@�@�@�@�@�@�@�@�@�@�@�@�@�x�]�����@�@�i�z���G�E�P���^�j
�L�b�Z�C��i�H�Ɗ������
�@�@��C�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�ێR�S�Ɓ@�@�i�}�����}�E���E���j
�@�@�i�����@������Ȋw�����Z���^�[�@�Ɖu�P�퐫�����`�[���@���C���i���������j�A
�@�@�@���l�s����w��w�@�@������Ȋw�����ȁ@�Ɖu�����w�������@��w�@���i���������j�j
�@�@�O���[�v�}�l�W���[�@�@�@�@�@�@�@�@�@���V�Y���@�@�i�I�I�T���E���E�X�P�j
�@�@��C�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@��؍F�K�@�@�i�X�Y�L�E�^�J���L�j
�@�@�������@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�R���T�q�@�@�i���}�E�`�E���E�R�j
�@�@�O���[�v�}�l�W���[�@�@�@�@�@�@�@�@�@���F��@�@�i�I�I�m�E�R�E�X�P�j
�@�@�O���[�v�}�l�W���[�@�@�@�@�@�@�@�@�@���m�j�@�@�i�C�m�E�G�E�q�g�V�j
�@�@�������@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�R�{���r�@�@�i���}���g�E�A�L�g�V�j
�@�@�����@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�с@�瓹�@�@�i�n���V�E�����~�`�j
�@�@�O���[�v�}�l�W���[�@�@�@�@�@�@�@�@�@�����T���@�@�i�I�N�n���E���E�W�j
�}�g��w�@��w��Ìn�@������Ȋw��@�P�~�J���o�C�I���W�[�@IT�n����
�@�@�����@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�L��M���@�@�i�q���J���E�^�J�c�O�j
�����x���@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�@�{�����͓��{��Ì����J���@�\�iAMED�j�����Ȋw�E�n����Վ��Ɓu�W�I�^���p�N���̍\��������g�����n�q�v�Z�p�̍��x���Ƒn��x���i������\�ҁF�L��M���AJP23ama121029j0001�j�v�A�Ȋw�Z�p�U���@�\�iJST�j�헪�I�n���������i����CREST�u�\���I�E���͊w�I��������p���������������w���̉�ǂƂ��̉��p�i������\�ҁF���ѓO��AJPMJCR2011�j�v�A���{�w�p�U����iJSPS�j�Ȋw����������Ɗ�Ռ����iB�j�u���ȖƉu�������ǂ�}�����鋹�B���זE�̋@�\�𐧌䂷��V�K�]�ʈ��q�̉�́i������\�ҁF�H�R�אg�A17H04038�j�v�u���B���זE�̑��l���ɂ�鎩�ȖƉu�����̔��Ǘ}���i������\�ҁF�H�R�אg�A20H03441�j�v�A����Ռ����iC�j�u���ȖƉu���e�ɕK�{�ȋ��B�������זE�֕������肷��]�ʈ��q�̓���Ƌ@�\��́i������\�ҁF�H�R�L�q�A17K08622�j�v�u���ȖƉu���e��U�����鋹�B���זE�̕����E�ێ��@�\�̉𖾁i������\�ҁF�H�R�L�q�A20K07332�j�v�̏����������̂ł��B